Кровь на hla типирование
Содержание:
Взаимозаменяемость однотипных тканей разных людей называется гистосовместимостью (от греч. hystos — ткань).
Гистосовместимость важна в первую очередь для пересадки органов и тканей другому человеку. Простейший пример — переливание крови, для которого нужно совпадение донора крови и реципиента (получателя) по системе AB0 и резус-фактору. Первоначально (в 1950-е годы) для пересадки органов ориентировались только на совместимость по эритроцитарным антигенам АВ0 и Rh. Это несколько улучшало выживаемость, но все равно давало слабые результаты. Перед учеными встала задача придумать что-то более действенное.
Что такое MHC и HLA
Чтобы избежать отторжения пересаженной ткани, органа или даже красного костного мозга, ученые стали разрабатывать систему генетического сходства у позвоночных животных и человека. Она получила общее название — Главный комплекс гистосовместимости (англ. MHC, Major Histocompatibility Complex).
Обратите внимание, что MHC является главным комплексом гистосовместимости, то есть он не единственный! Есть и другие системы, значимые для трансплантологии. Но в медвузах их практически не изучают.
Поскольку реакции отторжения осуществляются иммунной системой, то Главный комплекс гистосовместимости напрямую связан с клетками имунной системы, то есть с лейкоцитами. У человека главный комплекс гистосовместимости исторически называется Человеческим лейкоцитарным антигеном (обычно везде используется английское сокращение — HLA, от Human Leucocyte Antigen) и кодируется генами, расположенными в 6-й хромосоме.
Напомню, что антигеном называется химическое соединение (обычно белковой природы), которое способно вызывать реакцию иммунной системы (образование антител и др.), ранее я уже более подробно писал об антигенах и антителах.
Система HLA представляет собой индивидуальный набор различного типа белковых молекул, находящихся на поверхности клеток. Набор антигенов (HLA-статус) уникален для каждого человека.
К первому классу МНС относятся молекулы типов HLA-A, -B и -C. Антигены первого класса системы HLA находятся на поверхности ЛЮБЫХ клеток. Для гена HLA-А известны около 60 вариантов, для HLA-B — 136, а для гена HLA-С — 38 разновидностей.
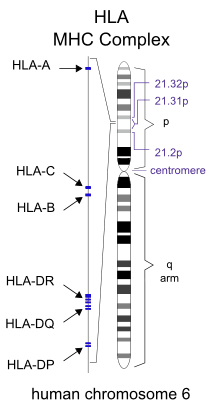
Расположение генов HLA в 6 хромосоме.
Источник рисунка: http://ru.wikipedia.org/wiki/Человеческий_лейкоцитарный_антиген
Представителями МНС второго класса являются HLA-DQ, -DP и -DR. Антигены второго класса системы HLA находятся на поверхности только некоторых клеток ИМУННОЙ системы (в основном это лимфоциты и макрофаги). Для транплантации ключевое значение имеет полная совместимость по HLA-DR (по другим HLA-антигенам отсутствие совместимости менее значимо).
HLA-типирование
Из школьной биологии надо помнить, что каждый белок в организме кодируется каким-либо геном в хромосомах, поэтому каждому белку-антигену системы HLA соответствует свой ген в геноме (наборе всех генов организма).
HLA-типирование — это выявление разновидностей HLA у обследуемого. У нас есть 2 способа определения (типирования) интересующих нас антигенов HLA:
1) с помощью стандартных антител по их реакции «антиген-антитело» (серологический метод, от лат. serum — сыворотка). С помощью серологического метода мы ищем белок-антиген HLA. HLA-антигены I класса для удобства определяют на поверхности Т-лимфоцитов, II класса — на поверхности В-лимфоцитов (лимфоцитотоксический тест).
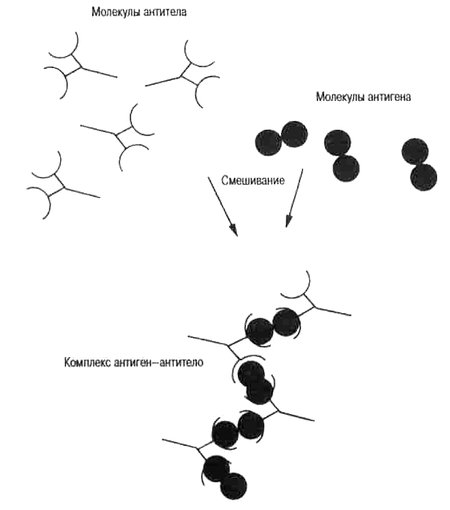
Схематическое изображение антигенов, антител и их реакции.
Источник рисунка: http://evolbiol.ru/lamarck3.htm
Серологический метод имеет много недостатков:
- нужна кровь обследуемого человека для выделения лимфоцитов,
- некоторые гены неактивны и не имеют соответствующих белков,
- возможны перекрестные реакции с похожими антигенами,
- искомые HLA-антигены могут быть в слишком низкой концентрации в организме или же слабо реагировать с антителами.
2) с помощью молекулярно-генетического метода — ПЦР (полимеразной цепной реакции). Мы ищем участок ДНК, который кодирует нужный нам антиген HLA. Для этого метода годится любая клетка организма, имеющая ядро. Зачастую достаточно взять соскоб со слизистой оболочки рта.
Наиболее точным является именно второй метод — ПЦР (оказалось, что некоторые гены системы HLA можно выявить только молекулярно-генетическим методом). HLA-типирование одной пары генов стоит 1-2 тыс. рос. рублей. При это сравнивают имеющийся вариант гена у пациента с контрольным вариантом этого гена в лаборатории. Ответ может быть положительным (совпадение найдено, гены идентичны) или отрицательным (гены разные). Для точного выяснения номера аллельного варианта обследуемого гена может понадобиться перебрать все возможные варианты (если помните, то для HLA-B их 136). Однако на практике никто не проверяет все аллельные варианты интересующего гена, достаточно подтвердить наличие или отсутствие только одного или нескольких наиболее значимых.
Итак, молекулярная система HLA (Human Leucocyte Antigens) кодируется в ДНК короткого плеча 6-й хромосомы. Там находится информация о белках, расположенных на клеточных мембранах и предназначенных для распознавания своих и чужеродных (микробных, вирусных и др.) антигенов и для координации клеток иммуннитета. Таким образом, чем больше сходства между двумя людьми по системе HLA, тем больше вероятность долгосрочного успеха при пересадке органа или ткани (идеальный случай — пересадка от однояйцевого близнеца). Однако изначальный биологический смысл системы MHC (HLA) состоит не в иммунологическом отторжении пересаженных органов, а заключается в обеспечении передачи белковых антигенов для распознавания различными разновидностями Т-лимфоцитов, ответственных за поддержание всех видов иммунитета. Определение HLA-варианта называется типированием.
В каких случаях проводят HLA-типирование?
Это обследование не является рутинным (массовым) и выполняется для диагностики только в сложных случаях:
- оценка риска развития ряда заболеваний с известной генетической предрасположенностью,
- выяснение причин бесплодия, невынашивания беременности (привычных выкидышей), иммунологической несовместимости.
HLA-B27
Типирование на HLA-B27 является, пожалуй, самым известным из всех. Этот антиген относится к MHC-I (молекулам главного комплекса гистосовместимости 1-го класса), то есть находится на поверхности всех клеток.
Согласно одной из теорий, молекула HLA–B27 хранит на себе и передает T-лифоцитам микробные пептиды (белковые микрочастицы), вызывающие артрит (воспаление суставов), что приводит к аутоиммунному ответу.
Молекула В27 способна участвовать в аутоиммунном процессе, направленном против собственных тканей организма, богатых коллагеном или протеогликанами (соединение белков с углеводами). Аутоиммунный процесс запускается бактериальной инфекцией. Наиболее частые бактериальные возбудители таковы:
- клебсиелла пневмонии,
- бактерии кишечной группы: сальмонелла, иерсиния, шигелла,
- хламидия (Chlamidia trachomatis).
У здоровых европейцев антиген HLA-B27 встречается всего в 8% случаев. Однако его наличие резко увеличивает (до 20-30%) шансы заболеть ассиметричным олигоартритом (воспаление нескольких суставов) и (или) получить поражение крестцово-подвздошного сочленения (воспаление соединения между крестцом и тазовыми костями).
Установлено, что HLA-B27 встречается:
- у больных анкилозирующим спондилоартритом (болезнью Бехтерева) в 90-95% случаев (это воспаление межпозвонковых суставов с последующим сращением позвонков),
- при реактивных (вторичных) артритах в 36-100% (аутоиммунно-аллергическое воспаление суставов после некоторых мочеполовых и кишечных инфекций),
- при болезни (синдроме) Рейтера в 70-85% (является разновидностью реактивного артрита и проявляется триадой, состоящей из артрита + воспаления мочевыводящего канала + воспаления слизистой оболочки глаз),
- при псориатическом артрите в 54% (артрит при псориазе),
- при энтеропатических артритах в 50% (артриты, связанные с поражением кишечника).
Если антиген HLA-B27 не обнаружен, болезнь Бехтерева и синдром Рейтера маловероятны, но в сложных случаях полностью исключить их все равно нельзя.
Если же у вас присутствует HLA-B27, советую вовремя лечить бактериальные кишечные инфекции и избегать половых инфекций (особенно хламидиоза), иначе с высокой вероятностью придется стать пациентом ревматолога и лечить воспаление суставов.
HLA-типирование для оценки риска сахарного диабета
Определенные разновидности HLA-антигенов чаще остальных встречаются у больных сахарным диабетом, а другие HLA-антигены — реже. Ученые пришли к выводу, что некоторые аллели (варианты одного гена) могут обладать провоцирующим или защитным действием при сахарном диабете. Например, наличие B8 или B15 в генотипе по отдельности увеличивает риск диабета в 2-3 раза, а совместно — в 10 раз. Присутствие определенных разновидностей генов может увеличивать риск заболевания сахарным диабетом 1 типа с 0,4% до 6-8%.
Счастливые носители B7 болеют диабетом в 14,5 раз реже тех людей, у которых B7 отсутствует. «Защитные» аллели в генотипе также способствуют более мягкому течению болезни в случае, если диабет все-таки разовьется (например, DQB*0602 у 6% больных СД 1 типа).

Экспрессия гена — это процесс использования генетической информации, при котором информация из ДНК превращается в РНК или белок.
HLA-типирование позволяет установить риск развития сахарного диабета 1 типа. Наиболее информативны антигены HLA II класса: DR3/DR4 и DQ. У 50% больных СД I типа обнаружены HLA-антигены DR4, DQB*0302 и/или DR3, DQB*0201. При этом риск развития болезни возрастает многократно.
(дополнение от 30 мая 2015)
HLA-антигены и невынашивание беременности
В комментариях здесь спросили:
У нас с мужем полное совпадение (6 из 6) по HLA второго типа. Есть ли способы бороться с невынашиванием беременности в таких случаях? К кому нужно обращаться, иммунологу?
Одним из иммунологических факторов невынашивания беременности является совпадение по 3 и более общим антигенам HLA II класса. Напомню, антигены HLA II класса находятся преимущественно на клетках иммунной системы (лейкоциты, моноциты, макрофаги, эпителиальные клетки). Ребенок получает половину генов от отца и половину от матери. Для иммунной системы любые белки, кодируемые генами, являются антигенами и потенциально способны вызывать иммунный ответ. В начале беременности (первый триместр) чужеродные для организма матери отцовские антигены плода вызывают у матери выработку защитных (блокирующих) антител. Эти защитные антитела связываются с отцовскими HLA-антигенами плода, защищая их от клеток иммунной системы матери (натуральных киллеров) и способствуя нормальному протеканию беременности.
Если же у родителей совпадает 4 и более антигена HLA II класса, то образование защитных антител резко снижается или не происходит. В этом случае развивающийся плод остается беззащитным от материнской иммунной системы, которая без защитных антител расценивает клетки эмбриона как скопление опухолевых клеток и старается их уничтожить (это естественный процесс, потому что в любом организме ежесуточно образуются опухолевые клетки, которые ликвидируются иммунной системой). В итоге наступает отторжение эмбриона и выкидыш. Таким образом, для для нормального протекания беременности нужно, чтобы супруги отличались HLA-антигенами II класса. Также существует статистика, какие аллели (варианты) HLA-генов женщин и мужчин приводят к выкидышам чаще или реже.
- Перед планируемой беременностью требуется вылечить инфекционно-воспалительные процессы у супругов, потому что наличие инфекции и воспаления активирует иммунную систему.
- В первой фазе менструального цикла (на 5-8 день) за 2-3 месяца до планируемого зачатия или программы ЭКО проводят лимфоцитоиммунотерапию (ЛИТ) лимфоцитами мужа (подкожно вводят лейкоциты отца будущего ребенка). Если муж болен гепатитом или другими вирусными инфекциями, используют донорские лимфоциты. Лимфоцитоиммунотерапия наиболее эффективна при наличии 4 и более совпадений по системе HLA и повышает шанс успешной беременности в 3-4 раза.
- Во второй фазе цикла (с 16 по 25 день) проводят лечение гормоном дидрогестероном.
- На ранних этапах беременности используют методы активной и пассивной иммунизации: лимфоцитоиммунотерапию каждые 3-4 недели до 12-14 недель беременности и внутривенное капельное введением средних доз иммуноглобулина (15 г в первом триместре). Это мероприятия способствуют успешному протеканию I триместра и снижают риск формирования плацентарной недостаточности.
Таким образом, лечение иммунологического невынашивания беременности должно проходить только в специализированном учреждении (центр невынашивания беременности, отделение патологии беременных и др.) под контролем штатного гинеколога, иммунолога, эндокринолога (гинеколога-эндокринолога). Обращаю внимание, что рядовые гинекологи и иммунологи из других медучреждений могут не иметь достаточной квалификации в этой области.
Ответ подготовлен на основе материала сайта http://bono-esse.ru/blizzard/Aku/AFS/abort_hla.html
P.S. (дополнение от 11 августа 2015)
Понятие женского иммунологического бесплодия сейчас подвергается сомнению, оно остается предметом научных споров и не рекомендуется к использованию в клинической практике. Подробнее см. комментарии ниже.
Материал был полезен? Поделитесь ссылкой:
комментария 2 к заметке «Что такое HLA и зачем нужно типирование по HLA»
26 Ноябрь, 2014 в 14:58
У меня много лет болят суставы, особенно на ногах, Последние годы вообще не могу толком ходить. Но все врачи из года в год говорят только одно: «Ну и что? У всех пожилых ноги болят. У нас тоже! Худеть надо!» Тем самым подозревают меня в излишнем нытье. И никто не посоветовал мне сдать кровь на HLA-B27! Я сама, занимаясь самолечением, сдала его платно и результат положительный. Теперь только врачи сочувственно замолчали! Безобразие! Что за медицина у нас.
11 Август, 2015 в 23:22
Я прочла эту статью и теперь хочу понять, где правда?
letidor.ru/article/hla_tri_zagadochnye_bukvy_30522/
HLA и бесплодие
Особенно популярно HLA-типирование в контексте «иммунологического бесплодия». Это и не удивительно, вопрос репродуктивной функции, реализации себя как родителя — очень важный и всегда глубоко эмоциональный. А значит, можно легко сыграть (и заработать) на этом. Есть данные, что от 10 до 36% беременностей прерываются спонтанно на ранних сроках у здоровых женщин в возрасте до 35 лет и после 42 соответственно. Если же беременность после ЭКО, то вероятность неудач еще выше. То есть, если прервалась одна или даже две подряд беременности, вне зависимости от их происхождения, — это не повод искать проблему. Тем более, это не повод говорить о «несовместимости» супругов.
Каково же происхождение этой теории? Исследования на экспериментальных животных в 60-х годах показали, что при спаривании сперматозоиды чаще соединяются с яйцеклеткой при выраженных различиях аллелей генов тканевой совместимости (HLA). В 70-х было обнаружено наличие антигенов HLA на поверхности сперматозоидов человека. Возникло предположение, что часть прервавшихся беременностей у человека связана с близкой гистосовместимостью супругов и были предложены терапевтические методы иммуномодуляции. Наиболее популярным подходом было переливание отмытых лимфоцитов мужа или донора до предполагаемой беременности или же, как вариант пассивной иммунизации, — внутривенное введение иммунноглобулинов (IVIG) в течение беременности.
На протяжении нескольких десятилетий европейские и американские врачи не просто следовали этим теориям, но обобщали свои результаты согласно правилам клинических исследований. Крупнейший мета-анализ 90-х годов (Ober C, et al. 1999) расставил все точки над i: это исследование включало 183 пациентки, было рандомизированным, проспективным, двойным слепым и многоцентровым (все условия достоверности!). Результат оказался потрясающим — в группе контроля, т.е. там где женщинам вводилось плацебо, эффективность «лечения» составила 48%, а в группе, получавших иммунотерапию — всего 36%. То есть, теория однозначно не подтвердилась.
На сегодня ведущие мировые рекомендации, основанные на доказательствах, гласят: «HLA — типирование, выявление цитотоксических антител против антигенов мужа и иммунотерапия не могут быть рекомендованы для обследования супружеских пар с невынашиванием беременности».
Это и понятно, учитывая то количество аллельных форм HLA-комплекса, о котором нам известно теперь. Реальное количество прервавшихся беременностей по иммунологической причине очень и очень мало. И даже если такой случай и был (хотя достоверно доказать его просто не возможно), это не является правилом для каждой беременности у данной пары. Поскольку вариантов комбинаций аллелей чрезвычайно много! И у следующего ребенка такая комбинация может быть даже очень благоприятной.
Так что, грустно наблюдать, как процветают не оправдавшиеся теории. И особенно если учесть, на основании каких анализов делают грандиозные выводы про HLA-совпадения. Практически невозможно провести полное HLA-генотипирование супругов, поскольку объем исследования был бы колоссален. Результаты, которые выдают в лабораториях, является очень приблизительным и очень усеченным вариантом типирования. Оценка совпадений генотипов супругов по таким результатам равноценна гаданию на кофейной гуще. И ладно бы ограничится громкой теорией про причину невынашивания, но главная опасность лишних анализов — лишнее псевдотерапевтическое вмешательство.
К началу 2000-х были детально проанализированы все иммунологические теории невынашивания и разные методы их коррекции. Вот окончательный вывод, основанный на многочисленных статистически достоверных исследованиях:
«Ни иммунизация лейкоцитами мужа, ни внутривенное введение иммуноглобулинов не увеличивает частоту родов у женщин с необъяснимыми повторными выкидышами. Такое лечение является дорогостоящими и имеет потенциально опасные побочные эффекты. Недопустимо подвергать женщин дополнительному чувству утраты, связанному с ложными ожиданиями от неэффективного лечения. Кроме того, лабораторные тесты, которые направлены на выявление показаний к иммунотерапии не имеют прогностического значения для исходов беременности и не должны применяться».
Давайте же прислушаемся к выводам, полученным тяжелым опытом других. Не будем наступать на те же грабли.
Комментарий автора сайта:
Скорее всего, ваша статья права. Согласно книге «Клинические аспекты лечения бесплодия в браке» (ГЭОТАР-Медиа, 2014), определять женские антиспермальные антитела и делать женщине иммунограмму не имеет смысла, потому что эти антитела встречаются с такой же частотой и у женщин с нормальной репродуктивной функцией. Понятие женского иммунологического бесплодия до сих пор остается предметом научных споров. Однако мужское иммунологическое бесплодие является научно доказанным и не подвергается сомнению. Для его диагностики делают MAR-тест, определяя процент сперматозоидов, покрытых мужскими антиспермальными антителами.

При неудачных попытках родить ребёнка супруги задаются вопросом — в чём причина? Первичные анализы и исследования часто не могут ответить на него. Для выявления проблемы врачи дополнительно назначают HLA-типирование пары. Иммунологическая идентичность родителей становится серьёзным препятствием на пути к рождению ребёнка.
Актуальность генетических анализов

Генетические анализы — наиболее современный метод выявления заболеваний и отклонений у человека
Вся информация о человеке, его особенностях развития, склонностях к заболеваниям зашифрована в молекуле ДНК. В настоящее время существуют сотни генетических тестов, позволяющих быстро выявить причину отклонений в здоровье и даже спрогнозировать их появление в будущем. В пренатальной диагностике такие анализы используются для раннего выявления наследственных заболеваний плода и «совместимости» супругов.
Типы и свойства HLA
HLA (Human Leucocyte Antigens), что в переводе с английского означает человеческий лейкоцитарный антиген, отвечает за реакцию гистологической совместимости. У нас всех есть свой набор HLA-молекул и HLA-генов. Дети получают половину HLA-генов от мамы и папы.
Самыми распространёнными являются «классические» и «неклассические» гены HLA. В данной статье для нас представляют интерес первые, а точнее, HLA II класса, основная функция которых сводится к антигенному распознаванию и межклеточному взаимодействию, обеспечению устойчивости человека к инфекциям. Но у них есть и минусы — они могут стать причиной аутоиммунных заболеваний и проблем во время беременности.
Роль HLA в протекании беременности
Для полноценного вынашивания ребёнка антигены отца и матери должны различаться. Зародыш, сформированный в результате соединения родительских половых клеток, обладает специализированными антигенами, «чужими» для иммунитета матери. Организм женщины реагирует на новые клетки ребёнка включением особых механизмов, защищающих плод: синтезируются антитела-протекторы, подавляющие специализированные NK-клетки-киллеры. Если этого не происходит, последние начинают убивать зародыш, что приводит к прерыванию беременности.
Если антигены отца и матери совпадают, то ребёнок будет носителем антигенов идентичных материнским. В таком случае женский организм считает клетки зародыша своими, а значит, не запускает защитные механизмы для сохранности плода. Иммунитет воспринимает плод как некое опухолевое заболевание и пытается его уничтожить или приостановить деление клеток. В обычной жизни это спасает нас от многих заболеваний, но в этом случае становится причиной некроза в тканях зародыша и приводит к выкидышу.
Комплекс гистосовместимости оказывает влияние на сам процесс оплодотворения, прикрепление зародыша и вынашиваемость плода. Существует прямая зависимость: чем больше аллелей HLA-генов оказалось схожим у супругов, тем больше риск выкидыша. Около 35% пар с повторяющимися случаями выкидыша имеют по 2–3 совпадения. Если обнаружено четыре и больше сходных аллелей, то невынашиваемость и безуспешные попытки ЭКО будут почти во всех случаях.
Для полноценного вынашивания плода очень важно не только количественное совпадение у родителей, но и сами аллели HLA-генов у каждого из супругов. Так, в парах с тремя и более выкидышами при расшифровке результатов NLA-типирования выявлено увеличение числа некоторых аллелей: у женщин – DQB1 0301, 0501, 0602; у мужчин – DRB1 10, 12; DQA1 0102, DQA1 0301, 0102; DQB1 0501, 0602. При повторяющихся выкидышах уменьшается частота аллелей DRB1 03 и DQB1 0303 как у женщин, так и у мужчин, что говорит об их защитном эффекте на течение беременности.
Показания к HLA-типированию
HLA-типирование не является стандартной процедурой при беременности. Этот тест назначают только в случаях с постоянным невынашиванием плода и при повторяющихся неудачах экстракорпорального оплодотворения.
Его проведение иногда рекомендовано только отцу, т. к. некоторые варианты антигенов приводят к отклонениям во время сперматогенеза и отрицательно сказываются на качестве половых клеток, что влияет на развитие плода.
Метод проведения
Полимеразная цепная реакция — высокоточный метод молекулярно-генетической диагностики
Для проведения генетического анализа супруги должны сдать кровь из вены. Из собранного материала будут выделены лейкоциты. Анализ проводят методом цепной полимеразной реакции (ПЦР). Врач-генетик на основе полученных результатов будет устанавливать степень иммунологической совместимости родителей.
Расшифровка результатов

В данном варианте у супругов 3 совпадения по вариантам HLA-антигенов
Полная иммунологическая несовместимость устанавливается, если у пары получен высокий процент совпадений ( пять и более из шести возможных в трёх локусах , имеющих по 2 варианта в каждом из локусов ) среди генов DRB1 , DQA1 , DQB1 . При частичной несовместимости результат не может быть назван главной причиной выкидышей. Полное несовпадение партнёров — положительный результат, идеальный для беспроблемного протекания беременности .
Иммунотерапия при совпадении анализов в паре
Методы сохранения беременности при иммунологической идентичности родителей были придуманы несколько десятилетий назад. Один из способов — вшивание ткани отца беременной женщине. Иммунитет начинал атаковать не плод, а инородные ткани. В дополнение проводилась чистка крови и подавление иммунитета матери.
Иммунизация — самый распространённый метод борьбы с HLA-идентичностью супругов
Сейчас возможны другие варианты поддержания беременности и защиты плода. После получения результатов лечащий врач может порекомендовать использовать иммунизацию. Существует два вида иммунизации — активная и пассивная.
- При активной женщине вводятся концентрированные лимфоциты супруга. Таким образом, организм будущей матери постепенно учится узнавать клетки мужа. Некоторые исследования приводят данные о 60% положительных результатов при вовремя проведённой процедуре.
- Пассивная иммунизация проводится специальными препаратами иммуноглобулинов (Октагам, Интраглобин, Иммуновенин и др.) Начинается процедура до зачатия, длится два — три месяца. Затем прописываются поддерживающие беременность курсы. Этот метод используется при экстракорпоральном оплодотворении.
Типирование HLA-генов супругов (видео)
Генетический анализ на HLA-антигенную совместимость супругов поможет выяснить, является ли бесплодие или невынашивание следствием генетической несовместимости пары. В случае подтверждения диагноза не теряйте надежду: современная медицина зачастую способна решить эту проблему и помочь в появлении на свет здорового малыша. Иммунизация матери является распространённым методом борьбы с генетической идентичностью родителей по HLA-антигенам.
Когда супруги долгое время не могут зачать ребенка, беременности заканчиваются выкидышами и ЭКО не дает результатов, супруги обращаются к репродуктологам. Бесплодие возникает по разным причинам, и одна из них — совпадение супругов по лейкоцитарным антигенам. Такое совпадение влечет за собой различные патологии, в том числе и хроническое невынашивание плода.

Понятие HLA-типирования и показания к назначению анализа
HLA – это человеческие лейкоцитарные антигены, или система тканевой совместимости человека. HLA является человеческим вариантом главного комплекса гистосовместимости. Его основное предназначение — регулирование работы иммунной системы. Гены, кодирующие HLA, расположены в 7 локусе 6 хромосомы. Этими генами кодируются атигенпредставляющие белки, расположенные на поверхности клеток.
Поскольку данные антигены определяют иммунитет, их необходимо учитывать при трансплантации органов. Игнорирование этого фактора приводит к отторжению пересаженного органа. HLA может уменьшать или увеличивать вероятность развития онкологических опухолей, вызывать появление аутоиммунных недугов.
Немалую роль система антигенов играет в выборе полового партнера. Проведенные в 1980-х гг. исследования показали, что женщины выбирают мужчин с отличающимся HLA. Комбинированные оральные контрацептивы подавляют биологический механизм выбора, и женщин, наоборот, начинают привлекать мужчины с одинаковым HLA.

Чем обусловлен такой выбор? Дело в том, что плод наследует комплекс антигенов от обоих родителей. Для успешного течения гестации важно, чтобы HLA у отца и матери был разным и, как следствие, отличался у матери и эмбриона. Если окажется, что система совместимости у беременной женщины и у ребенка одинаковая, организм матери воспримет тело эмбриона как свои клетки. Иммунная система решит, что это не чужеродный организм, а опухоль, новообразование, и будет атаковать клетки эмбриона.
Совпадение HLA приводит к хроническому невынашиванию, выкидышам, в том числе при ЭКО. Невозможность выносить ребенка является прямым показанием к диагностике лейкоцитарных антигенов, которая называется HLA-типированием.
Классы HLA-типирования и их отличия
Существуют 2 класса HLA:
- І класс — кодируют гены на локусах А, В, С. Эти антигены представляют собой пептиды — фрагменты белков, разрушенных в протеасомах. Они расположены на поверхности всех клеток, кроме эритроцитов и трофобластов. Если в организм попадает клетка с чужеродным антигеном, к ней стекаются Т-киллеры и уничтожают ее. Наличие некоторых антигенов этого класса вызывает заболевания. Например, если у человека есть антиген В27, то у него разовьются спондилит и синдром Рейтера. Молекула В27 включает аутоиммунные процессы против своего же организма, а запускают ее активность бактериальные инфекции: хламидии, сальмонеллы, шигеллы, клебсиеллы.
- II класс — кодируют гены на локусах DP, DM, DOA, DOB, DQ, DR. Расположены на поверхностях дендритных клеток, макрофагов и В-лимфоцитов. Доказано, что инсулинзависимый сахарный диабет появляется у людей с антигенами DR3, DR4.

Как проводится анализ?
Существуют 2 способа проведения анализа на HLA:
- серологический;
- молекулярно-генетический.
При серологическом методе у обследуемого берут кровь и соединяют ее с сывороткой. По тому, выделяются ли антитела, определяется присутствие HLA-антигенов в крови. Этот метод имеет ряд неудобств. Некоторые гены могут оказаться неактивными и не иметь соответствующих им белков, могут быть в слишком низкой концентрации. К тому же возможна перекрестная реакция с другими антигенами.
Второй метод использует полимеразную цепную реакцию и является наиболее точным. Врач-генетик находит и сравнивает нужные участки хромосомы, которые кодируют ген. Каждый ген имеет несколько аллелей — вариантов, которые могут совпадать с аллелями другого человека или нет. Для анализа подойдет любая клетка тела, обычно берут мазок со слизистой оболочки полости рта.
Иногда биоматериал сдает не пара, а только будущий отец. Это объясняется тем, что некоторые аллели влияют на спермограмму, изменяют вид сперматозоидов, их подвижность и жизнеспособность.

Специальной подготовки перед диагностикой не требуется. Супруги обращаются в лабораторию в удобный для них день, сдают биоматериал и ждут результатов. Обычно результаты готовы через 6 рабочих дней.
Расшифровка результатов
Составлением и расшифровкой результатов анализа на HLA-типирование занимаются врач-генетик и врач-иммунолог. По окончании исследования составляют таблицу, куда вносят информацию об обнаруженных аллелях. Сначала генетик вносит буквенно-цифровые кодировки генов: DRB1, DQA1, DQB1, а затем добавляет цифры, шифрующие аллели, причем первые две цифры кодируют номер группы аллелей гена, а остальные две — вариант гена. У взрослых людей при расшифровке DRB1 имеет значение номер группы аллелей, а при расшифровывании остальных — номер варианта.
Совпадение по двум аллелям увеличивает вероятность выкидыша до 35%. При совпадении 4 аллелей супруги считаются полностью несовместимыми для деторождения.
Что делать супругам, у которых совпадают HLA? Врачи предлагают лечить бесплодие с помощью иммунизации:
- Активная иммунизация. Женщине вводят лимфоциты мужа – так ее организм привыкает к другим клеткам и учится их распознавать.
- Пассивная иммунизация. Этот метод используют при экстракорпоральном оплодотворении. За 2-3 месяца врачи-репродуктологи назначают специальные препараты: Октагам, Интраглобин, Иммуновенин. Эти лекарства содержат человеческий иммуноглобулин, который повышает содержание антител в организме.

Где можно сдать анализ, сколько это стоит?
Где можно сделать типирование? HLA-типирование — это сложный анализ, который требует применения специального оборудования. Не в каждой больнице есть генетическая лаборатория и специалисты, обладающие необходимыми знаниями. Супругам придется искать специализированные клиники, которые занимаются генетической диагностикой и репродуктивными технологиями.
Сколько стоит анализ? Стоимость HLA-типирования немаленькая и зависит от того, какой конкретно класс антигенов будет исследоваться. HLA-типирование ІІ класса стоит в среднем 5 000-7 000 руб. на одного человека. Следует учитывать, что дополнительно оплачиваются анализ крови и консультация врача-генетика, которая может стоить 1 500-2 500 руб. Еще дороже стоит лечение – цена на лекарства для пассивной иммунизации может доходить до 35 000 руб.
К анализу на HLA-типирование следует прибегать в последнюю очередь. Сначала необходимо исключить другие возможные причины бесплодия и только потом делать генетический анализ.
