Маркеры внутриутробных инфекций
Содержание:
Со времени открытия серологических маркеров инфекций данный анализ является основным в лабораторных исследованиях. Цель его проведения – помощь в распознавании заболеваний инфекционного происхождения, а также выявление недугов, обусловленных нарушением защитных функций иммунной системы.
Диагностирование гепатитов, краснухи, сифилиса, ВИЧ и многих других болезней в наше время стало доступно благодаря анализам на серологические маркеры инфекций. Расшифровка результатов исследований помогает достаточно быстро определить наличие заболеваний, которые иногда бывает трудно выявить обычными способами.
Серологический метод исследования: помощь врачу в определении природы заболеваний

Анализ свойств и эффектов сывороток
Происхождение наименования «серология» — от лат. названия сыворотки (serum). Сочетание с известным logos означает «учение о сыворотке». Под серологией подразумевается раздел иммунологии, изучающий специфику взаимодействия антител сыворотки с антигенами.
Основа серологической диагностики – выявление специфических антител, образующихся в ответ на инфицирование определенным антигеном. По наличию в крови определенных антител делается заключение о характере и степени активности инфекции.
Серологический метод используется в диагностике:
- герпеса
- кишечных инфекций
- цитомегаловируса
- эпидемического паротита
- атипичной пневмонии
- краснухи
- хламидиоза
- токсоплазмоза
- сифилиса
- ВИЧ
- кори
- вирусных гепатитов В и C
Исследование применяют и в случаях, когда требуется выявление причин миокардитов.
Серологические реакции могут быть применены:
- В случае если нужно подтвердить диагноз. Практикуется добавление в сыворотку крови соответствующего антигена. Наличие антител доказывается либо опровергается характером ответной реакции.
- В случае, когда о характере заболевания ничего не известно, видовая принадлежность антигенов, находящихся в крови, выявляется добавлением антител.
Для проведения анализа из крови предварительно удаляют компонент, ответственный за свертываемость (фиброген).
Таким образом, цель проведения серологического анализа крови:
- Постановка диагноза. Исследование показано в случае, когда требуется лабораторное подтверждение присутствия в сыворотке крови возбудителя.
- Назначение лечения. Анализ поможет выявить реакцию возбудителя на различные лекарства.
Использование серологического анализа практикуется и при диагностике аутоиммунных заболеваний. Проведение процедуры помогает выявить антитела к тканям организма.
Серологические маркеры гепатитов: расшифровки результатов

Вирусные гепатиты относятся к тому виду серьёзных инфекционных заболеваний, которые могут достаточно долго протекать, ничем себя особенно не проявляя. В трудности своевременного обнаружения и заключается его главная опасность.
Проведение анализа на маркеры, появляющиеся в крови как следствие введения вакцины или перенесенного заболевания, позволяет выявить гепатит в ранней фазе, в которой он лучше поддается излечению.
Виды вирусных гепатитов
Гепатит А
Этот вид (так называемая желтуха) встречается достаточно часто. Передается при употреблении инфицированных продуктов и воды. При его диагностике анализ делается на наличие антител:
- Аnti-НАV IgМ. Существование в крови ранних антител свидетельствует о наличии вируса в организме не менее 25-30 дней.
- Аnti-НАV IgG. Его наличие – свидетельство того, что пациент переболел данной формой гепатита в прошлом.
Гепатит В
Передается половым путем. Вирус может попасть в кровь и при использовании нестерильных инструментов. Распространен широко, при своевременном выявлении хорошо поддается лечению. По выздоровлении организм приобретает к вирусу пожизненный иммунитет. Нелеченый гепатит В, вероятнее всего, перейдет в хроническую форму, которая грозит осложнениями в виде цирроза и рака печени.
При выявлении гепатита В ищут следующие маркеры:
- HВsAg. Специфический антиген, показывающий наличие заболевания.
- Аnti-НВs. Его появление свидетельствует о завершении процесса.
- Аnti-НВс IgG. Его длительное нахождение в организме указывает на течение процесса.
- Аnti-НВс IgM. Его обнаружение является признаком начальной фазы заболевания.
- Аnti-НВе. Его присутствие – признак вялотекущей формы гепатита.
Гепатит С
Наиболее тяжёлая форма заболевания. Поддается лечению лишь на ранних стадиях. Исход несвоевременно выявленной болезни – летальный.
По результатам исследований выявляются следующие маркеры:
- Аnti-НСV. Свидетельствует о наличии заболевания.
- Аnti-НСV IgM. Позволяет судить о достаточно недавнем заражении, что дает основания для благоприятного прогноза.
Гепатит D
Симптоматика та же, что и у гепатита В. Диагностируется присутствием аnti-НDV Ig G, характерного для гепатита В, дополненного аnti-НDV Ig M.
Гепатит Е
В целом подобен гепатиту А, но более опасен для беременных. Выявляется присутствием anti-HEV lg.
Гепатит G
По свойствам близок к гепатиту С, но менее опасен.
Маркеры внутриутробных инфекций: интерпретация результатов

Необходимые анализы во время беременности
Беременность – период, когда подверженность инфекциям становится достаточно острой проблемой для организма. Существует группа инфекций, которые опасны для беременных, в то время как для остальных групп пациентов не представляет угрозы. Названа эта группа ТОRСН-инфекциями. Название образовано из первых букв входящий в группу названий инфекций:
- токсоплазмоз
- другие инфекции (сифилис, листериоз, хламидиоз и др.)
- краснуха
- цитомегаловирусная инфекция
- герпес
Выявленные антитела IgG означают наличие иммунитета к заболеванию. Препятствием для планирования беременности не являются.
Обнаружение IgM возможно лишь в острой стадии. Беременность можно планировать лишь после выздоровления.
Краснуха. Относится к инфекциям, передающимся внутриутробно. Перенесенное заболевание формирует пожизненный иммунитет. Тяжесть, с которой протекает заболевание, прямо пропорциональна возрасту больного. У плода инфицированной женщины велика вероятность развития тяжелых пороков. Сегодня есть возможность привиться от краснухи, тем самым избежав вероятности заболеть во время беременности. После прививки в течение некоторого времени в крови сохраняются титры IgM, поэтому от планирования беременности лучше воздержаться в течение 3 мес.
Перед прививкой нужно сделать серологический анализ, после которого можно принимать решение о проведении прививки.
- IgМ-, IgG-: обозначает отсутствие антител и необходимость вакцинации.
- IgМ-, IgG+: показывает наличие иммунитета. Вакцинация не требуется.
- IgМ+, IgG-: заболевание в ранней стадии, период обострения.
- IgМ+, IgG+: период обострения.
Динамика отслеживается по степени понижения IgM и увеличения IgG. Заболевание опасно в острой фазе при положительном значении IgM.
Появление в крови IgM либо IgG, если ранее их у данной пациентки не наблюдалось, означает развитие заболевания. Такой же вердикт можно вынести при 4-кратном повышении за две-три недели количества IgG. Срок давности предыдущего обследования также имеет значение: антитела могут присутствовать в крови в течение 2 лет от начала заболевания. Поэтому наличие IgM не может интерпретироваться как признак острой инфекции. Наличие IgG в снижающемся количестве – не считается заболеванием и не представляет опасности.
Если заражение произошло во II или III триместре, заболевание излечимо.
Безопасный анализ: серологическое исследование при аллергии

Диагностические анализы при аллергии проводят с помощью количественного определения иммуноглобулина Е. При этом способе аллергены связываются с антителами, образуя единый комплекс. В исследовании используется более 200 аллергенов.
Более тщательные исследования проводятся, когда нужно выявить тип и степень остроты реакции. Преимущество этого метода заключается в отсутствии прямого контакта пациента с аллергеном. При этом определяются общие и аллергенспецифические IgE.
В определении диагноза важны не только лабораторные исследования, но и другие данные. Сопоставить их и правильно диагностировать наличие заболевания может только врач, специализирующийся в данной области. Самолечением на основании расшифровки серологических анализов заниматься нельзя.
Заметили ошибку? Выделите ее и нажмите Ctrl+Enter, чтобы сообщить нам.

Одной из важнейших проблем современной перинатологии является прогрессирующий рост инфекционной патологии у плода и новорожденного. В структуре заболеваемости новорожденных внутриутробные инфекции (ВУИ) занимают второе место после гипоксии и асфиксии в родах [4].
В структуре перинатальной смертности удельный вес ВУИ достигает 65,6% [11]. В настоящее время насчитывается более 2500 возбудителей, способных вызывать внутриутробное инфицирование плода, при этом количество их постоянно пополняется [14]. Чаще диагностируется смешанное инфицирование вирусно-бактериальной, вирусно-вирусной природы и их различные ассоциации с трихомонадами и дрожжевыми грибами рода Candida [12].
Возбудители этих инфекций обладают прямым и непрямым действием на фето-плацентарную систему. Дегтярев Д.Н. и соав. (1998) утверждают, что чем меньше гестационный возраст плода, тем более выражена альтерация тканей. В результате этого основным клиническим проявлением инфекции плода, возникающих на ранних сроках беременности являются пороки развития [2]. По мере увеличения сроков беременности в клинической картине инфекционного заболевания плода начинают преобладать симптомы классического системного воспаления, обусловленные выраженной пролиферацией и экссудацией, что проявляется в виде гепатита, пневмонии менингита, энтероколита и других заболеваний [6].
Непрямое воздействие возбудителей на фето-плацентарную систему приводит к таким осложнениям беременности как угроза прерывания, внутриутробная гипоксия плода, ЗВУР, метаболические нарушения без специфических клинически признаков ВУИ [8-9].
Учитывая неспецифичность клинических проявлений ВУИ во время беременности, диагностика ее затруднена и возможна лишь в результате сочетания клинических и лабораторно-инструментальных методов исследования [5]. Метод ультразвуковой диагностики является доступным, высоко информативным, не инвазивным и позволяет провести эхографическую оценку структурной патологии плода, плаценты, амниона, а также определить степень гемодинамических нарушений фето-плацентарного комплекса у беременных с высоким инфекционным индексом [3,12].
Целью данной работы является комплексная эхографическая характеристика функциональной системы «мать — плацента — плод» при внутриутробном инфицировании, что необходимо для оптимизации тактики ведения беременной, а также позволит прогнозировать степень тяжести внутриутробного инфицирования у новорожденного.
Материалы и методы
Под наблюдением находились 123 беременных женщины, которым проводились все необходимые клинико-лабораторные обследования, а также ультразвуковое исследование в сроке 30-36 недель гестации. В зависимости от выраженности ВУИ и степени тяжести состояния все новорожденные разделены на 4 клинические группы.
1 группа (n=40) — контрольная, новорожденные от матерей с неосложненной беременностью, состояние ребенка при рождении удовлетворительное. 2-я группа (n=30) — состояние ребенка при рождении удовлетворительное или средней степени тяжести с локальными проявлениями ВУИ в виде пиодермии, ринита, отита, конъюнктивита, пневмонии. 3-я группа (n=25) — состояние ребенка при рождении тяжелое или средней степени тяжести с ухудшением в раннем неонатальном периоде с локальными формами ВУИ в виде пневмонии, энтероколита, менингита, фетального гепатита и др. заболеваний. 4-я группа (n=28) — состояние ребенка при рождении тяжелое или крайней степени тяжести с генерализованными или локальными проявлениями ВУИ, потребовавшими проведения искусственной вентиляции легких. Матери детей 2-4 групп имели высокий инфекционный индекс.
Таблица 1.
Комплексное ультразвуковое исследование фетоплацентарной системы включало в себя: определение биофизического профиля плода, допплерометрическое исследование, оценку параметров кардиотокографии, что осуществлялось на аппарате «LOGIQ 5 EXPERT» по общепринятой методике. Биофизический профиль плода оценивали по шкале А.М. Vintzeleos et al.,1983, включающей следующие параметры: дыхательное движение, двигательную активность, тонус плода, объем околоплодных вод, структуру плаценты, нестрессовый тест.
Фетометрия позволила установить соответствие размеров плода гестационному сроку, диагностировать задержку внутриутробного развития.
При исследовании сердечной деятельности плода использовали шкалу Фишера, 1976., основными показателями которой были: базальная частота сердечных сокращений, амплитуда осцилляций, частота осцилляций, акцелерации, децелерации. Критерии состояния плода следующие: 8 — 10 баллов — нормальное состояние; 5 — 7 баллов — сомнительное; 0 — 4 балла — неудовлетворительное.
Таблица 2. Заболеваемость беременных урогенитальными инфекциями
Диагностическими критериями нарушения маточно-плацентарного и плодово-плацентарного кровотока при доношенной беременности считали следующие числовые значения СДО: в артерии пуповины 3,0 и выше, а также нулевые и отрицательные значения диастолического кровотока; в маточных артериях 2,4 и выше; в аорте плода 8,0 и выше; для средней мозговой артерии менее 4 и более 7 у.е. [10].
Для оценки степени нарушений маточно-плацентарно-плодовой гемодинамики пользовались шкалой А.Н. Стрижакова (1991).
I А степень — изолированное нарушение кровотока в маточных артериях; I Б степень — изолированное нарушение кровотока в артерии пуповины; II степень — сочетанное нарушение кровотока в маточных артериях и артерии пуповины; III степень — критическое нарушение плодового кровотока, характеризующееся нулевым или ретроградным диастолическим компонентом в артерии пуповины.
Результаты исследований
На основании ранее проведенных исследований [1] выделяют 3 группы эхографических маркеров внутриутробного инфицирования: 1) маркеры внутри-утробного инфицирования плаценты (плацентит); 2) маркеры внутриутробного инфицирования околоплодных вод (амнионит); 3) маркеры внутриутробного
инфицирования плода (инфекционные фетопатии).
По данным ультразвукового исследования структурной организации плаценты получены следующие результаты. В контрольной (первой) группе нарушения зарегистрированы у 4 (10%) женщин, из них у 2 (5%) отмечалось преждевременное созревание плаценты, которое регистрировалось с 33 недель, и у 2 (5%) — расширение межворсинчатого пространства, что связано с низким артериальным давлением в период плацентации. Сочетания признаков не отмечалось. Во второй клинической группе преждевременное созревание плаценты зарегистрировано в 5 (16,6%) случаях, увеличение толщины плаценты в 2 (6,6%) случаях, расширение межворсинчатого пространства в 6 (20%) случаях. В 4 (13,3%) случаях отмечалось сочетание признаков. В третьей клинической группе преждевременное созревание плаценты выявлено у 9 (36%) женщин, а незрелость плаценты (I степень) у 2 (8%) женщин. Увеличение толщины плаценты отмечалось у 6 (24%) женщин, расширение межворсинчатого пространства у 9 (36%) женщин. Сочетание признаков наблюдалось в 12 (48%) случаях. В 4 клинической группе преждевременное созревание плаценты отмечалось у 12 (42,8%) женщин, незрелость плаценты у 5 (17,8%) женщин, увеличение толщины плаценты у 10 (35,7%) женщин, расширение межворсинчатого пространства у 15 (53,6%) женщин. Количество сочетания признаков увеличилось до 19 (67,8%) случаев, причем, наиболее частыми сочетаниями были преждевременное созревание плаценты и расширение межворсинчатого пространства (вне зависимости от клинических групп). Кроме того, в 4 группе у 6 (21,4%) пациентов плацента была кистозно изменена, в двух случаях (7,1%) отмечено формирование псевдокист.
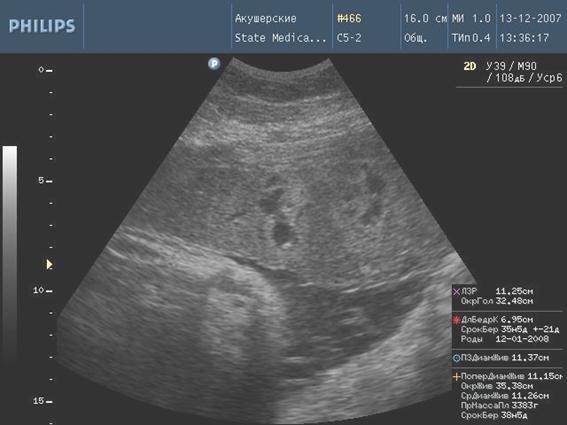
Рис. 1. Формирование псевдокист
При оценке объема и качества околоплодных вод были выявлены следующие закономерности. В контрольной группе данная патология определялась у 6 (15%) пациентов, из них у 1 (2,5%) в виде умеренно выраженного маловодия, у 2 (5%) — в виде умеренно выраженного многоводия, гиперэхогенные включения в околоплодных водах зарегистрированы у 3 (7,5%) пациентов. Сочетания признаков не выявлено. В основных группах патология околоплодных вод обнаружена у 63 (75,9%) пациентов. Так, во 2 клинической группе маловодие выявлено у 6 (20%) женщин, многоводие — у 2 (6,6%) женщин, гиперэхогенные включения отмечались у 8 (26,6%) женщин. Сочетание признаков зарегистрировано в 5 (16,6%) случаях. В 3 клинической группе маловодие наблюдалось в 11 (44%) случаях, многоводие в 5 (20%) случаях, гиперэхогенные включения в 9 (36%) случаях. Кроме того, в 2 (8%) случаях было зарегистрировано наличие амниотических тяжей, свободно располагающихся в амниотической полости. В 4 клинической группе маловодие выявлено у 18 (64,3%) беременных, многоводие у 7 (25%) беременных; наличие гиперэхогенных включений и амниотических тяжей в 12 (42,8%) и 4 (14,3%) случаях соответственно. Кроме того, в основных группах многоводие с множественными гиперэхогенными включениями сочеталось в 26 (31,3 %) случаях, у 4 (4,8 %) беременных многоводие сочеталось с амниотическими тяжами.
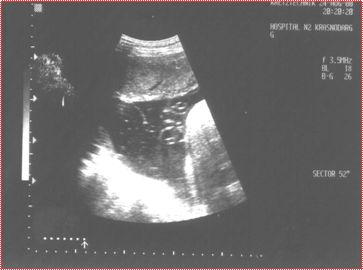
Рис. 2. Эхографический маркер внутриутробного инфицирования околоплодных вод (свободно расположенный амниотический тяж)
При ультразвуковом исследовании у плодов с инфекционными фетопатиями обнаружены следующие эхографические особенности. Расширение чашечно-лоханочной системы выявлено у 4 (14,3%) плодов 4-ой группы и у 2 (8%) плодов третьей группы (рис. 3), вентрикуломегалия у 4-х (14,3%) плодов 4 группы и у 2 (8%) плодов 3 группы (рис. 4), гепатомегалии у 5 (17,8%) плодов 4 группы и у 2 (8%) плодов в 3 группе. Кардиомегалия с гидроперикардом зарегистрированы у 2-х (7,1%) плодов 4 группы. Отмечено появление линейных гиперэхогенных включений в перивентрикулярных зонах головного мозга плода в 4 (14,3%) случаях в 4 клинической группе, в 2 (8%) случаях в 3 клинической группе и в 1 (3,3%) случае во 2 группе. Кисты в сосудистых сплетениях головного мозга плода обнаружены в 2 (7,1%) случаях в 4 группе, в 1 (4%) случае в 3 группе и в 1 (3,3%) случае во 2 группе. Патологическое расширение петель толстого кишечника зарегистрировано у 2 (7,1%) плодов 4 группы и у 1 (4%) плода в 3 группе. Асцит выявлен у 1 (3,6%) плода 4 группы. Таким образом, наибольшее число инфекционных фетопатий было выявлено у беременных 4 клинической группы.
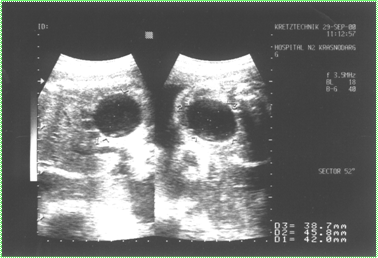
Рис. 3. Эхографический маркер внутриутробного инфицирования плода (правосторонняя пиелоэктазия)
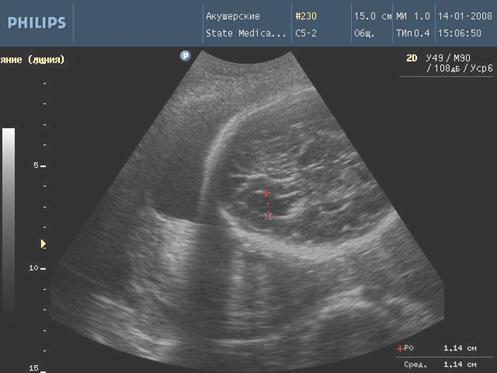
Рис. 4. Вентрикуломегалия
ЗВУР плода зарегистрирована в 29 случаях (34,9%) в основных группах и в 1 (2,5%) случае в контрольной группе. Во 2 клинической группе ЗВУР I-II степени выявлена у 7 (23,3%) плодов. В 3 клинической группе ЗВУР диагностирована у 8 (32%) плодов, из них у 5 (20%) зарегистрирована ЗВУР плода I степени, у 2 (8%) — II степени, у 1 (4%) — III степени. В 4 клинической группе количество случаев ЗВУР плода увеличилось до 14 (50%), причем ЗВУР I степени отмечалась у 8 (28,6%) плодов, ЗВУР II степени — у 4 (14,3%) плодов, ЗВУР III степени у 2 (7,1%) плодов.
Исследования биофизической активности плода выявили следующие результаты. При оценке дыхательной активности плода в 1 клинической группе максимальная продолжительность одного эпизода дыхательных движений более 60 секунд определена у 35 (87,5%) плодов. У 5 (12,5%) отмечалось снижение дыхательной активности, из них у 4 (10%) продолжительность составила от 30 до 60 сек. и у 1 (2,5%) отмечалось резкое снижение данного параметра. В этой группе адекватная двигательная активность сохранялась у 38 (95%) плодов, небольшое снижение двигательной активности зарегистрировано у 2 (5%) плодов. Тонус у плодов был удовлетворительным в 100% случаев.
Во 2 клинической группе снижение дыхательной активности наблюдалось у 14 (46,6%) плодов, из них у 2 (6,6%) она не регистрировалась вообще. Снижение тонуса и двигательной активности отмечалось одномоментно у 3 (10%) плодов.
В 3 клинической группе снижение дыхательной активности наблюдалось у 16 (64%) плодов, из них у 11 (44%) продолжительность одного эпизода дыхательных движений составила от 30 до 60 сек., а у 5 (20%) плодов — менее 30 сек. В 4 группе в 82,1% случаев отмечалось снижение дыхательной активности, у 9 (32,1%) плодов — резкое снижение данного параметра. Тонус и двигательная активность плода являются наиболее точными маркерами тяжести внутриутробного страдания плода. Так в 3 клинической группе снижение данных показателей отмечалось у 17 (68%) плодов, в 4 группе — у 25 (89,2%) плодов, причем отсутствие общей двигательной активности за время наблюдения определялось у 6 (24%) плодов 3 группы и у 15 (53,5%) плодов 4 группы.
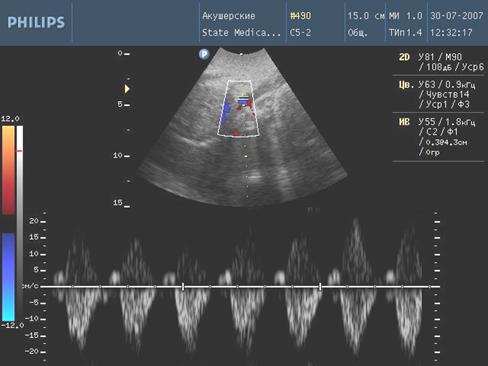
Рис. 5. Нарешение гемодинамики III ст. (ретроградный кровоток)
С целью изучения особенностей гемодинамических нарушений в фетоплацентарном комплексе у беременных с высоким инфекционным индексом были использованы значения систоло-диастолического отношения (СДО) в маточных артериях, артерии пуповины и средней мозговой артерии.
Таблица 3. Средние значения СДО в изучаемых сосудах

Внутриутробные инфекции – группа заболеваний плода и новорожденного, развивающихся вследствие заражения в дородовом периоде или в родах. Внутриутробные инфекции могут приводить к гибели плода, самопроизвольному аборту, задержке внутриутробного развития, преждевременным родам, формированию врожденных пороков, поражению внутренних органов и ЦНС. Методы диагностики внутриутробных инфекций включают микроскопические, культуральные, иммуноферментные, молекулярно-биологические исследования. Лечение внутриутробных инфекций проводится с использованием иммуноглобулинов, иммуномодуляторов, противовирусных, антибактериальных препаратов.

Общие сведения
Внутриутробные инфекции – патологические процессы и заболевания, обусловленные антенатальным и интранатальным инфицированием плода. Истинная распространенность внутриутробных инфекций не установлена, однако, согласно обобщенным данным, с врожденными инфекциями рождается не менее 10% новорожденных. Актуальность проблемы внутриутробных инфекций в педиатрии обусловлена высокими репродуктивными потерями, ранней неонатальной заболеваемостью, приводящей к инвалидизации и постнатальной гибели детей. Вопросы профилактики внутриутробных инфекций лежат в плоскости рассмотрения акушерства и гинекологии, неонатологии, педиатрии.

Причины внутриутробных инфекций
Внутриутробные инфекции развиваются в результате инфицирования плода в дородовом периоде или непосредственно во время родов. Обычно источником внутриутробной инфекции для ребенка выступает мать, т. е. имеет место вертикальный механизм передачи, который в антенатальном периоде реализуется трансплацентарным или восходящим (через инфицированные околоплодные воды) путями, а в интранатальном — аспирационным или контактным путями.
Реже происходит ятрогенное инфицирование плода в период беременности при проведении женщине инвазивной пренатальной диагностики (амниоцентеза, кордоцентеза, биопсии ворсин хориона), введении плоду препаратов крови через сосуды пуповины (плазмы, эритроцитарной массы, иммуноглобулинов) и т. д.
В антенатальном периоде инфицирование плода обычно связано с вирусными агентами (вирусами краснухи, герпеса, цитомегалии, гепатита В и С, Коксаки, ВИЧ) и внутриклеточными возбудителями (токсоплазмоза, микоплазмоза).
В интранатальном периоде чаще происходит микробная контаминация, характер и степень которой зависит от микробного пейзажа родовых путей матери. Среди бактериальных агентов наиболее распространены энтеробактерии, стрептококки группы В, гонококки, синегнойная палочки, протей, клебсиелла и др. Плацентарный барьер непроницаем для большинства бактерий и простейших, однако при повреждении плаценты и развитии фетоплацентарной недостаточности, может произойти антенатальное микробное инфицирование (например, возбудителем сифилиса). Кроме этого, не исключается и интранатальное вирусное заражение.
Факторами возникновения внутриутробных инфекций служат отягощенный акушерско-гинекологический анамнез матери (неспецифические кольпиты, эндоцервициты, ЗППП, сальпингофориты), неблагополучное течение беременности (угроза прерывания, гестозы, преждевременная отслойка плаценты) и инфекционная заболеваемость беременной. Риск развития манифестной формы внутриутробной инфекции существенно выше у недоношенных детей и в том случае, когда женщина инфицируется первично во время беременности.
На тяжесть клинических проявлений внутриутробной инфекции влияют сроки инфицирования и вид возбудителя. Так, если инфицирование происходит в первые 8-10 недель эмбриогенеза, беременность обычно заканчивается самопроизвольным выкидышем. Внутриутробные инфекции, возникшие в раннем фетальном периоде (до 12 недели гестации), могут приводить к мертворождению или формированию грубых пороков развития. Внутриутробное инфицирование плода во II и III триместре беременности проявляется поражением отдельных органов (миокардитом, гепатитом, менингитом, менингоэнцефалитом) либо генерализованной инфекцией.
Известно, что тяжесть проявлений инфекционного процесса у беременной и у плода может не совпадать. Бессимптомное или малосимптомное течение инфекции и у матери может вызвать тяжелые поражения плода, вплоть до его гибели. Это связано с повышенным тропизмом вирусных и микробных возбудителей к эмбриональным тканям, преимущественно ЦНС, сердца, органа зрения.
Классификация
Этиологическая структура внутриутробных инфекций предполагает их деление на:
- вирусные (вирусный гепатит, герпес, краснуха, ОРВИ, цитомегалия, эпидемический паротит, энтеровирусная инфекция)
- бактериальные (туберкулез, сифилис, листериоз, сепсис)
- паразитарные и грибковые (микоплазмоз, токсоплазмоз, хламидиоз, кандидоз и др.)
Для обозначения группы наиболее распространенных внутриутробных инфекций используется аббревиатура TORCH-синдром, объединяющий токсоплазмоз (toxoplasmosis), краснуху (rubella), цитомегалию (cytomegalovirus), герпес (herpes simplex). Буквой О (other) обозначаются другие инфекции, в числе которых — вирусные гепатиты, ВИЧ-инфекция, ветряная оспа, листериоз, микоплазмоз, сифилис, хламидиоз и др.).
Симптомы внутриутробных инфекций
Наличие внутриутробной инфекции у новорожденного может быть заподозрено уже во время родов. В пользу внутриутробного инфицирования может свидетельствовать излитие мутных околоплодных вод, загрязненных меконием и имеющих неприятный запах, состояние плаценты (полнокровие, микротробозы, микронекрозы). Дети с внутриутробной инфекцией часто рождаются в состоянии асфиксии, с пренатальной гипотрофией, увеличенной печенью, пороками развития или стигмами дисэмбриогенеза, микроцефалией, гидроцефалией. С первых дней жизни у них отмечается желтуха, элементы пиодермии, розеолезных или везикулезных высыпаний на коже, лихорадка, судорожный синдром, респиратрные и кардиоваскулярные расстройства.
Ранний неонатальный период при внутриутробных инфекциях нередко отягощается интерстициальной пневмонией, омфалитом, миокардитом или кардитом, анемией, кератоконъюнктивитом, хориоретинитом, геморрагическим синдромом и др. При инструментальном обследовании у новорожденных могут обнаруживаться врожденная катаракта, глаукома, врожденные пороки сердца, кисты и кальцификаты мозга.
В перинатальном периоде у ребенка отмечаются частые и обильные срыгивания, мышечная гипотония, синдром угнетения ЦНС, серый цвет кожных покровов. В поздние сроки при длительном инкубационном периоде внутриутробной инфекции возможно развитие поздних менингитов, энцефалитов, остеомиелита.
Рассмотрим проявления основных внутриутробных инфекций, составляющих TORCH-синдром.
Врождённый токсоплазмоз
Внутриутробное инфицирование одноклеточным протозойным паразитом Toxoplasma Gondii приводит к тяжелым поражениям плода – задержке развития, врожденным порокам развития мозга, глаз, сердца, скелета.
После рождения в остром периоде внутриутробная инфекция проявляется лихорадкой, желтухой, отечным синдромом, экзантемой, геморрагиями, диареей, судорогами, гепатоспленомегалией, миокардитом, нефритом, пневмонией. При подостром течении доминирую признаки менингита или энцефалита. При хронической персистенции развивается гидроцефалия с микроцефалией, иридоциклит, косоглазие, атрофия зрительных нервов. Иногда встречаются моносимптомные и латентные формы внутриутробной инфекции.
К числу поздних осложнений врожденного токсоплазмоза относятся олигофрения, эпилепсия, слепота.
Врождённая краснуха
Внутриутробная инфекция возникает из-за заболевания краснухой при беременности. Вероятность и последствия инфицирования плода зависят от гестационного срока: в первые 8 недель риск достигает 80%; последствиями внутриутробной инфекции могут служить самопроизвольное прерывание беременности, эмбрио- и фетопатии. Во II триместре риск внутриутробного инфицирования составляет 10-20%, в III – 3-8%.
Дети с внутриутробной инфекцией обычно рождаются недоношенными или с низкой массой тела. Для периода новорожденности характерна геморрагическая сыпь, длительная желтуха.
Классические проявления врожденной краснухи представлены триадой Грега: поражением глаз (микрофтальмией, катарактой, глаукомой, хориоретинитом), ВПС (открытым артериальным протоком, ДМПП, ДМЖП, стенозом легочной артерии), поражением слухового нерва (сенсоневральной глухотой). В случае развития внутриутробной инфекции во второй половине беременности у ребенка обычно имеется ретинопатия и глухота.
Кроме основных проявлений врожденной краснухи, у ребенка могут выявляться и другие аномалии: микроцефалия, гидроцефалия, расщелины нёба, гепатит, гепатоспленомегалия, пороки развития мочеполовой системы и скелета. В дальнейшем внутриутробная инфекция напоминает о себе отставанием ребенка в физическом развитии, ЗПР или умственной отсталостью.
Врождённая цитомегалия
Внутриутробное заражение цитомегаловирусной инфекцией может приводить к локальному или генерализованному поражению многих органов, иммунодефициту, гнойно-септическим осложнениям. Врожденные дефекты развития обычно включают микроцефалию, микрогирию, микрофтальмию, ретинопатию, катаракту, ВПС и др. Неонатальный период врожденной цитомегалии осложняется желтухой, геморрагическим синдромом, двусторонней пневмонией, интерстициальным нефритом, анемией.
К отдаленным последствиям внутриутробной инфекции относятся слепота, нейросенсорная глухота, энцефалопатия, цирроз печени, пневмосклероз.
Врождённая герпетическая инфекция
Внутриутробная герпес-инфекция может протекать в генерализованной (50%), неврологической (20%), слизисто-кожной форме (20%).
Генерализованная внутриутробная врожденная герпетическая инфекция протекает с выраженным токсикозом, респираторным дистресс-синдромом, гепатомегалией, желтухой, пневмонией, тромбоцитопенией, геморрагическим синдромом. Неврологическая форма врожденного герпеса клинически проявляется энцефалитом и менингоэнцефалитом. Внутриутробная герпес-инфекция с развитием кожного синдрома сопровождается появлением везикулярной сыпи на кожных покровах и слизистых оболочках, в т. ч. внутренних органов. При наслоении бактериальной инфекции развивается сепсис новорожденных.
Внутриутробная герпес-инфекция у ребенка может приводить к формированию пороков развития — микроцефалии, ретинопатии, гипоплазии конечностей (кортикальной карликовости). В числе поздних осложнений врожденного герпеса — энцефалопатия, глухота, слепота, задержка психомоторного развития.
Диагностика
В настоящее время актуальной задачей является пренатальная диагностика внутриутробных инфекций. С этой целью на ранних сроках беременности проводится микроскопия мазка, бактериологический посев из влагалища на флору, ПЦР-исследование соскоба, обследование на TORCH-комплекс. Беременным из группы высокого риска по развитию внутриутробной инфекции показана инвазивная пренатальная диагностика (аспирация ворсин хориона, амниоцентез с исследованием амниотической жидкости, кордоцентез с исследованием пуповинной крови).
Возможно выявление эхографических маркеров внутриутробных инфекций с помощью акушерского УЗИ. К косвенным эхографическим признакам внутриутробного инфицирования относятся маловодие или многоводие; наличие гиперэхогенной взвеси в околоплодных водах или амниотических тяжей; гипоплазия ворсин хориона, плацентит; преждевременное старение плаценты; отечный синдром плода (асцит, перикардит, плеврит), гепатоспленомегалия, кальцификаты и пороки развития внутренних органов и др. В процессе допплерографического исследования кровотока выявляются нарушения плодово-плацентарного кровотока. Кардиотокография обнаруживает признаки гипоксии плода.
После рождения ребенка с целью достоверной верификации этиологии внутриутробной инфекции используются микробиологические (вирусологические, бактериологические), молекулярно-биологические (ДНК-гибридизация, ПЦР), серологические (ИФА) методики обследования. Важное диагностическое значение имеет гистологическое исследование плаценты.
По показаниям новорожденные с внутриутробными инфекциями в первые сутки жизни должны быть осмотрены детским неврологом, детским кардиологом, детским офтальмологом и др. специалистами. Целесообразно провести ЭхоКГ, нейросонографию, офтальмоскопию, исследование слуха методом вызванной отоакустической эмиссии.
Лечение внутриутробных инфекций
Общие принципы лечения внутриутробных инфекций предполагают проведение иммунотерапии, противовирусной, антибактериальной и посиндромной терапии.
Иммунотерапия включает применение поливалентных и специфических иммуноглобулинов, иммуномодуляторов (интерферонов). Противовирусная терапия направленного действия осуществляется, главным образом, ацикловиром. Для противомикробной терапии бактериальных внутриутробных инфекций используются антибиотики широкого спектра действия (цефалоспорины, аминогликозиды, карбапенемы), при микоплазменной и хламидийной инфекциях – макролиды.
Посиндромная терапия внутриутробных инфекций направлена на купирование отдельных проявлений перинатального поражения ЦНС, геморрагического синдрома, гепатита, миокардита, пневмонии и т. д.
Прогноз и профилактика
При генерализованных формах внутриутробных инфекций летальность в неонатальном периоде достигает 80%. При локальных формах возникают серьезные поражения внутренних органов (кардиомиопатии, ХОБЛ, интерстициальный нефрит, хронический гепатит, цирроз и т. д.). Практически во всех случаях внутриутробные инфекции приводят к поражению ЦНС.
Профилактика внутриутробных инфекций заключается в проведении предгравидарной подготовки, лечении ЗППП до наступления беременности, исключении контактов беременной с инфекционными больными, коррекции программы ведения беременности у женщин групп риска. Женщины, ранее не болевшие краснухой и не получавшие прививки против краснухи, должны быть вакцинированы не позднее, чем за 3 месяца до предполагаемой беременности. В ряде случаев внутриутробные инфекции могут являться основанием для искусственного прерывания беременности.
